Im Bereich der mRNA-Impfstoffe und Nukleinsäuretherapien dienen Lipidnanopartikel (LNPs) als zentrale Träger für die effiziente Nukleinsäureverabreichung. Die Lipidmaterialien sind dabei entscheidend für die Effizienz und Biosicherheit der LNP-Verabreichung. Aufgrund der inhärenten Instabilität von mRNA mussten LNP-Formulierungen jedoch lange Zeit bei niedrigen Temperaturen gelagert werden. Die während der Gefrier-Tau-Zyklen entstehenden Eiskristalle und osmotischen Belastungen können leicht zur Aggregation der LNPs und zum Austritt von mRNA führen und somit deren praktische Anwendung stark einschränken.
Ein Team des Instituts für Chemie der Chinesischen Akademie der Wissenschaften veröffentlichte in Nature Communications Forschungsergebnisse, die eine neuartige Lösung vorschlagen: die Nutzung des Gefrierkonzentrationseffekts zur aktiven Einbindung von Betain-basierten Kryoprotektiva (CPAs) in Lipidnanopartikel (LNPs). Dieser Ansatz erhält nicht nur die Stabilität der Formulierung, sondern verbessert auch die mRNA-Transfektionseffizienz signifikant. Die Studie eröffnet neue Perspektiven für die Optimierung lipidbasierter Formulierungen.

Forschungshintergrund
mRNA ist sehr empfindlich gegenüber Hydrolyse, Oxidation und enzymatischem Abbau, weshalb sie zur Stabilisierung tiefgekühlt gelagert werden muss. Klinisch eingesetzte mRNA-Impfstoffe wie mRNA-1273 und BNT162b2 verwenden Saccharose als Kryoprotektivum. Trotz Kryoprotektiva bestehen jedoch während der Gefrier-Auftau-Zyklen zwei zentrale Probleme:
-
Störung der physikalischen Stabilität: Die Bildung von Eiskristallen und osmotische Druckänderungen können zur Verschmelzung und Aggregation von LNP führen und dadurch deren sphärische Struktur und Größenhomogenität beeinträchtigen.
-
Verminderte Liefereffizienz: Strukturelle Schäden an LNPs können zu mRNA-Leckagen und einer geschwächten endosomalen Freisetzung führen, was letztendlich die Effizienz der mRNA-Expression in Zielzellen verringert.
Während sich die bisherige Forschung hauptsächlich auf die "passive Stabilisierung" von LNPs konzentriert, nutzt diese Studie innovativ den Gefrier-Auftau-Prozess selbst, um Kryoprotektiva von bloßen "Stabilisatoren" in "funktionelle Verstärker" umzuwandeln und so eine doppelte Verbesserung der Stabilität und der Freisetzungseffizienz zu erzielen.
Gefrierkonzentration treibt die Integration von BT-CPA in LNPs voran
Das Forschungsteam entwickelte ein zusammengesetztes Kryoprotektivum (BT-CPA) aus Betain und Trehalose. In einer Reihe von Experimenten wiesen sie nach, dass das Einfrieren die aktive Einlagerung von BT-CPA in Lipidnanopartikel (LNPs) bewirkt und dadurch zwei wichtige Effekte erzielt: (1) Erhalt der strukturellen Integrität der LNPs nach Gefrier-Auftau-Zyklen und (2) Verbesserung der Fähigkeit der LNPs, aus Endosomen freigesetzt zu werden, wodurch die Effizienz der mRNA-Übertragung gesteigert wird.
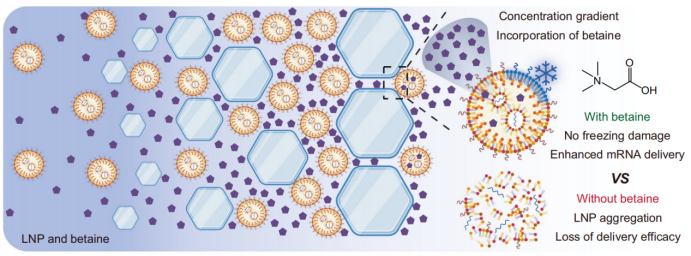
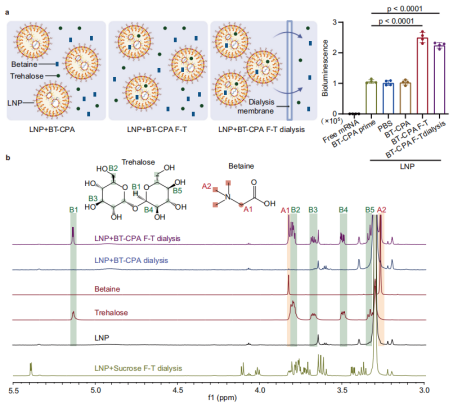
Beim Gefrieren bilden sich Eiskristalle im Wasser, wodurch die Konzentrationen von LNPs und Kryoprotektiva in der verbleibenden flüssigen Phase stark ansteigen – ein Phänomen, das als „Gefrierkonzentration“ bezeichnet wird. Dieser Prozess erzeugt einen steilen Konzentrationsgradienten über die LNP-Membran, der die passive Diffusion von Betain und Trehalose in das Innere der LNPs durch vorübergehende Lücken in der Lipidmembran (verursacht durch mechanische Spannungen von Eiskristallen und Lipidphasenübergängen) antreibt.
Die Forscher validierten diesen Mechanismus mittels Protonen-Kernspinresonanz (¹H-NMR) und hochauflösender Massenspektrometrie: In LNP+BT-CPA-Proben, die Gefrier-Auftau-Zyklen unterzogen wurden, waren charakteristische Signale von Betain (Peaks bei 3,28 ppm und 3,83 ppm) und Trehalose (z. B. Peak bei 3,34 ppm) selbst nach Dialyse zur Entfernung von freiem BT-CPA nachweisbar. Im Gegensatz dazu zeigten LNP+BT-CPA-Proben, die keinen Gefrier-Auftau-Zyklen unterzogen wurden, nur eine minimale BT-CPA-Einkapselung. Dies bestätigt, dass das Einfrieren für den Einbau von BT-CPA in LNPs über die einfache Oberflächenadsorption hinaus notwendig ist.
Optimierung von BT-CPA: Präzise Kontrolle von Konzentration und Verhältnis
Um Stabilität und Verabreichungseffizienz in Einklang zu bringen, optimierten die Forscher systematisch die BT-CPA-Konzentration und das Verhältnis:
-
Optimierung des Mischungsverhältnisses: Die alleinige Verwendung von 25 mg/ml Betain erhielt die Stabilität der LNP aufrecht, die mRNA-Verkapselungseffizienz war jedoch etwas geringer als mit 87 mg/ml Saccharose. Die Zugabe von 25 mg/ml Trehalose (d. h. BT-CPA: 25 mg/ml Betain + 25 mg/ml Trehalose) führte zu minimalen Veränderungen der LNP-Größe nach dem Einfrieren und Auftauen, einer stabilen mRNA-Verkapselungseffizienz und einer 1,4-fachen Steigerung der Freisetzungseffizienz im Vergleich zu Betain allein sowie einer 2,4-fachen Steigerung gegenüber frischen LNP.
-
Konzentrationsschwelleneffekt: Eine Erhöhung der Betainkonzentration von 10 mg/ml auf 25 mg/ml steigerte die mRNA-Transfereffizienz signifikant, eine weitere Erhöhung auf 75 mg/ml führte jedoch zu keinem zusätzlichen Gewinn, sodass 25 mg/ml als optimale Konzentration festgelegt wurde.
-
Optimierung des Gefrier-Auftau-Zyklus: 1–2 Zyklen erhöhten die Freisetzungseffizienz, ohne die LNP-Struktur zu beschädigen, während 6 Zyklen zu LNP-Aggregation, mRNA-Leckage und verringerter Effizienz führten, wodurch 2 Zyklen als optimal identifiziert wurden.
BT-CPA verbessert die mRNA-Abgabe durch Förderung des endosomalen Escape.
Mithilfe zellulärer Experimente und mechanistischer Validierung konnten die Forscher klären, dass BT-CPA die Effizienz der Wirkstofffreisetzung nicht durch Beeinflussung der zellulären Aufnahme verbessert, sondern durch die Steigerung des endosomalen Austritts, um die mRNA-Expression zu erhöhen.
-
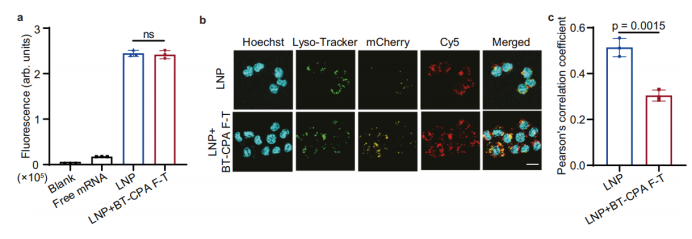
Unveränderte zelluläre Aufnahme, verstärkter endosomaler Escape: Die Durchflusszytometrie zeigte, dass die zelluläre Aufnahmeeffizienz von mit BT-CPA behandelten und gefriergetrockneten SM-102-LNPs (BT-CPA-LNPs) nahezu identisch mit der von frischen SM-102-LNPs war. Die Konfokalmikroskopie ergab jedoch eine signifikant reduzierte Überlappung zwischen Cy5-markierter mRNA (rot) und lysosomalen Markern (grün) in BT-CPA-LNPs mit einem signifikant niedrigeren Pearson-Korrelationskoeffizienten (PCC) als bei frischen LNPs, was auf einen verstärkten endosomalen Escape hindeutet.
-
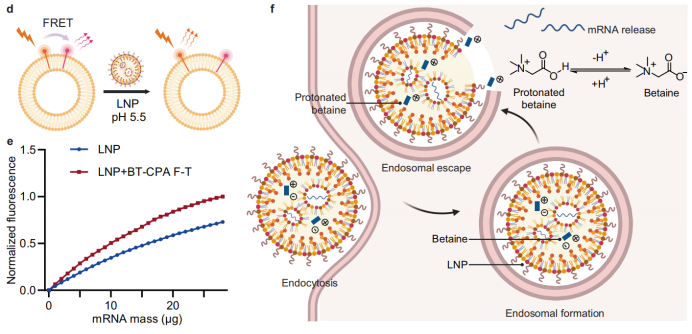
Molekularer Mechanismus: Betainprotonierung vermittelt Membranfusion: Betain, ein zwitterionisches Molekül, wird im sauren endosomalen Milieu protoniert, wodurch es positiv geladen wird und elektrostatische Wechselwirkungen mit negativ geladenen endosomalen Membranen fördert, was die Fusion erleichtert. Membranfusionsversuche mit NBD-PE- und Rhod-PE-markierten Modellendosomen zeigten eine stärkere Fluoreszenzlöschung von NBD in BT-CPA-LNPs, was eine erhöhte Fusionsfähigkeit bestätigt.
-
Universalität: Kompatibilität mit verschiedenen Lipiden: Die verstärkende Wirkung von BT-CPA beschränkt sich nicht auf SM-102, sondern gilt für verschiedene klinisch verwendete ionisierbare Lipide (z. B. ALC-0315, MC3). Mit diesen Lipiden hergestellte LNPs zeigten nach BT-CPA-Behandlung und Gefrier-Auftau-Zyklen eine signifikant verbesserte mRNA-Transfer-Effizienz mit Partikelgrößen unter 200 nm und einem PDI < 0,2, was ein breites Anwendungsspektrum belegt.
In-vivo-Validierung: Stärkere Immunantwort und Dosisersparnisvorteil
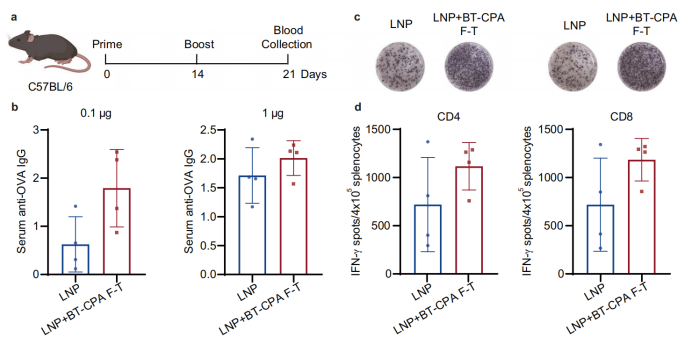
Bei C57BL/6-Mäusen zeigten BT-CPA-LNPs signifikante Vorteile:
-
Höhere mRNA-Expression: 4 h und 24 h nach intramuskulärer Injektion war die Luciferase-Expression in BT-CPA-LNPs 2,3-fach bzw. 1,7-fach höher als in frischen LNPs.
-
Stärkere Immunantwort: BT-CPA-LNPs, die Ovalbumin-mRNA (mOVA) einkapseln, induzierten bei Dosen von 0,1 μg und 1 μg signifikant höhere OVA-spezifische IgG-Antikörpertiter, und ELISpot-Assays zeigten eine Zunahme von IFN-γ-positiven CD4⁺- und CD8⁺-T-Zellen.
-
Ausgezeichnete Langzeitstabilität: Nach 6 Monaten bei -80°C wiesen BT-CPA-LNPs eine hohe mRNA-Expressionseffizienz bei geringer Zytotoxizität auf (DC2.4-Zellviabilität > 90%).
Bedeutung der Forschung
Diese Studie schlägt nicht nur eine neuartige Kryoprotektionsstrategie für LNP vor, sondern definiert Kryoprotektiva auch als „aktive Komponenten“, die während des Einfrierens in LNP eingebaut werden können, um deren Funktion zu regulieren. Zu den wichtigsten Beiträgen gehören:
-
Optimierung von Lagerprotokollen: Bewältigung von Stabilitätsproblemen bei der Lagerung und dem Transport von LNP bei niedrigen Temperaturen, Unterstützung der globalen Verteilung von mRNA-Impfstoffen und Nukleinsäure-Arzneimitteln.
-
Erweiterung der Lipidanwendungen: Nachweis, dass Lipide wie SM-102, ALC-0315 und MC3 durch BT-CPA eine verbesserte Verabreichung erreichen können, was Anwendungen in der Krebsimmuntherapie und Gentherapie unterstützt.
-
Innovative Formulierungsentwicklung: Pionierarbeit beim Konzept der „Nutzung des Gefrierens zur Funktionsverbesserung“ und damit ein neues Paradigma für die Entwicklung von LNP.
Abschluss
Durch die strategische Nutzung des Gefrierprozesses wandelt diese Forschung die Herausforderungen der LNP-Lagerung in funktionelle Vorteile um und bietet eine wertvolle technische Lösung zur Optimierung der Formulierungen von Kernlipiden wie SM-102, ALC-0315 und MC3 mit vielversprechenden Auswirkungen auf die Behandlung von Krankheiten.
SINOPEG liefert die in der Studie verwendeten Lipide (SM-102, ALC-0315, MC3) und bietet Liposomen-Hilfsstoffe aus einer Hand sowie eine Reihe firmeneigener Lipid-Hilfsstoffe. Darüber hinaus liefern wir hochwertige Polysaccharide und polyzwitterionische Produkte für vielfältige Forschungs- und Entwicklungs- sowie Produktionsanforderungen.
Referenz
Cheng X, Zheng X, Tao K, et al. Durch Gefrieren induzierter Einbau von Betain in Lipidnanopartikel verbessert die mRNA-Übertragung. Nature Communications. 2025;16(1):4700.
Über uns
SINOPEG bietet effiziente Komplettlösungen für die Beschaffung in den Bereichen Arzneimittelverabreichung, Biopharmazeutika und Materialwissenschaften.
Technologieplattformen und Kernprodukte:
-
Pharmazeutische/medizinische PEG-Derivate: Lineare und strukturierte PEGs (mehrarmig, V-förmig, Y-förmig usw.).
-
Fettsäure-Seitenkettenmodifikatoren: Semaglutid-, Liraglutid-, Tirzepatid-Seitenketten und Peptidlinker.
-
Lipid (LNP) Plattform: Umfassende mRNA-Impfstoff-LNP-Lipide, einschließlich proprietärer kationischer Lipide.
-
ADC/ProTAC Linker-Plattform: Standard- und kundenspezifische Linker.
-
Blockcopolymer-Plattform: Makromolekulare Mizellen als Wirkstoffträger.
Unsere nach ISO9001/13485/14001/45001, EcoVadis und GB/T29490 zertifizierten Einrichtungen entsprechen den cGMP-Standards und den ICH-Q7A-Richtlinien und gewährleisten so qualitativ hochwertige Produkte und Dienstleistungen für Kunden weltweit.