Im Bereich der Biomedizin erlebt die CAR-T-Zelltherapie einen revolutionären Sprung von der In-vitro-Präparation zur In-vivo-Programmierung. Das Jahr 2025 markiert einen entscheidenden Wendepunkt in der Entwicklung der In-vivo-CAR-T-Zelltherapie. Im Juni gab Capstan bekannt, dass seine auf dem tLNP-Vektor basierende In-vivo-CAR-T-Zelltherapie CPTX2309 offiziell in die Phase-I-Studie eingetreten ist. Anschließend erwarb AbbVie Capstan für 2,1 Milliarden US-Dollar in bar und sicherte sich damit die firmeneigene tLNP-Plattformtechnologie. Diese Transaktion belegt die hohe Anerkennung der In-vivo-CAR-T-Zelltherapie durch führende Pharmaunternehmen und markiert den offiziellen Übergang dieser Technologie vom Machbarkeitsnachweis in eine neue Phase der klinischen Entwicklung.

In-vivo-CAR-T-Zellen und tLNP: Der nächste Trend in der Präzisionsmedizin
Branchenhintergrund: Ein revolutionärer Sprung von In-vitro- zu In-vivo-Studien
Die traditionelle CAR-T-Zelltherapie in vitro hat bei B-Zell-Leukämie und Lymphomen bemerkenswerte Fortschritte erzielt. Ihr komplexer Herstellungsprozess, die hohen Kosten und die Toxizität stellen jedoch Hürden für die breite Anwendung dieser Technologie dar. Laut Branchenstudien kann der Preis eines kommerziellen CAR-T-Zellprodukts zwischen 370.000 und 470.000 US-Dollar liegen, und von der Zellgewinnung bis zur Reinfusion vergehen drei bis fünf Wochen. Manche Patienten können aufgrund des raschen Fortschreitens ihrer Erkrankung nicht so lange warten.
Die In-vivo-CAR-T-Zelltherapie, ein revolutionärer technologischer Ansatz, schleust CAR-Gene mithilfe spezieller Vektoren direkt in den Körper ein. Dadurch werden die aufwendigen In-vitro-Schritte umgangen und die „Aufrüstung“ der T-Zellen direkt im Körper des Patienten durchgeführt. Dieses „In-Body-Fabrik“-Modell vereinfacht nicht nur den Behandlungsprozess erheblich, sondern soll auch die Kosten auf ein Zehntel der Kosten herkömmlicher CAR-T-Zelltherapien senken und damit einen Durchbruch für die nächste Generation der zellulären Immuntherapie darstellen.
tLNP: Das zentrale Verabreichungssystem für in vivo CAR-T
Im Rahmen der Implementierung der CAR-T-Zelltherapie in vivo haben sich zielgerichtete Lipidnanopartikel (tLNP) als Standardverfahren in der Industrie etabliert. tLNP verleihen herkömmlichen LNP die Fähigkeit, Genmaterial präzise zu erkennen und an T-Zellen abzugeben, indem ihre Oberfläche mit spezifischen Zielmolekülen (wie Antikörpern und Peptiden) modifiziert wird.
Die Kerntechnologie besteht in der präzisen Kopplung des zielgerichteten Antikörpers an die Oberfläche der Lipidnanopartikel (LNP), wodurch ein „navigationsraketenartiges“ Transportsystem entsteht. Gelangt die tLNP in den Körper, lenkt der zielgerichtete Ligand auf der Oberfläche das gesamte Nanopartikel gezielt zu T-Zellen und schleust CAR-mRNA durch Endozytose in die Zellen ein, wodurch eine In-situ-Reprogrammierung der T-Zellen erreicht wird.
DSPE-PEG-MAL
Die entscheidende „chemische Brücke“ für den Aufbau von tLNP
Gezielte Auslieferung vorantreiben: Dreifache Stärkung der tLNP-Funktionalisierung
Im komplexen System der tLNP-Herstellung spielt DSPE-PEG-MAL eine dynamische „Ausführerrolle“. Sein Strukturdesign entspricht präzise seinen Schlüsselfunktionen im Herstellungsprozess, und seine Rolle lässt sich in die folgenden drei aufeinander aufbauenden und zusammenhängenden Schritte unterteilen.
• Einbettung und Verankerung: Präzise Positionierung von der Lösung bis zur Membranphase
Während der Selbstassemblierung von LNP kann sich DSPE-PEG-MAL aufgrund der physikochemischen Eigenschaften seines hydrophoben DSPE-Schwanzes spontan an die entstehende Lipiddoppelschichtmembran anlagern. Dadurch wird sichergestellt, dass das gesamte Molekül in einer vorgegebenen Orientierung und stabil in die LNP-Struktur integriert wird und somit die Grundlage für nachfolgende Funktionen bildet.
• Dehnung und Schutz: Räumliche Verteidigungslinien an der Schnittstelle errichten
Nach der Verankerung dehnen sich die hydrophilen PEG2000-Ketten vollständig in die wässrige Umgebung der LNP aus und bilden eine flexible, hydratisierte, bürstenartige Schutzschicht. Diese Schutzschicht dient als erste Verteidigungslinie für die LNP und erhält deren physikochemische Stabilität und funktionelle Integrität im komplexen In-vivo-Milieu aufrecht, indem sie die unspezifische Proteinadsorption hemmt und die Partikelaggregation reduziert. Dadurch wird die Halbwertszeit im Körper verlängert.
• Klick und Ermächtigung: Die chemische Transformation von allgemeinen Trägerraketen zu Präzisionsraketen
Die Maleimidgruppe (-MAL) am Ende der PEG-Kette ist der chemische Schalter, der LNP „Intelligenz“ verleiht. Als hochselektive Biokopplungsstelle kann sie effizient mit den Thiolgruppen von gentechnisch veränderten Antikörpern reagieren (beispielsweise eingeführt durch Reduktion von Disulfidbrücken oder mithilfe von Reagenzien wie SATA). Genau durch diesen irreversiblen kovalenten Bindungsschritt werden gewöhnliche LNPS „aktiviert“ und entwickeln sich zu zielgerichteten TLNPS, die spezifische Zelloberflächenantigene präzise erkennen können.
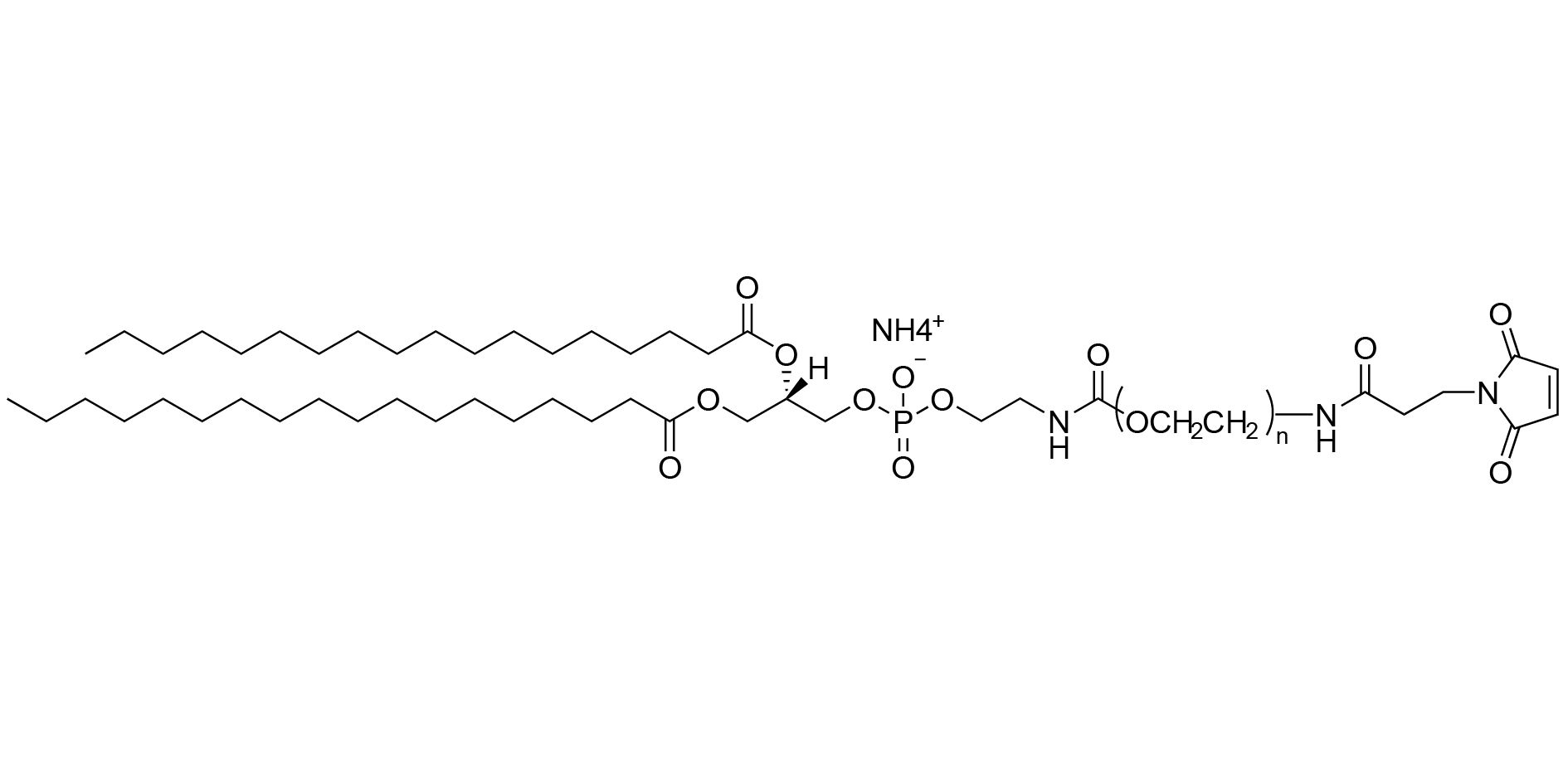
Abbildung 1: Schematische Darstellung der Molekülstruktur von DSPE-PEG-MAL (Ammoniumsalz)
Der technische Ansatz zur Erzielung einer Antikörperkonjugation auf der Oberfläche von LNP
Die Verwendung von DSPE-PEG-MAL zur Antikörperkonjugation auf der Oberfläche von LNP ist derzeit die ausgereifteste und am weitesten verbreitete Strategie zur Herstellung von tLNP. Dieser Prozess umfasst üblicherweise drei Kernschritte:
Herstellung von LNP: DSPE-PEG-MAL wird mittels mikrofluidischer Mischtechnologie mit anderen Lipidkomponenten (ionisierbaren Lipiden, Hilfslipiden, Cholesterin, PEG-Lipiden) vermischt, um LNP herzustellen. Dabei wird die Maleimidgruppe (-MAL) von DSPE-PEG-MAL an der Oberfläche der LNP exponiert.
2. Antikörper-Vorbehandlung: Gemäß den in der Industrie üblichen Methoden zur Herstellung zielgerichteter LNPS (wie sie beispielsweise von Capstan Therapeutics im Patent WO2024249954 beschrieben werden) werden die Antikörper mit Thiol (-SH) modifiziert, um sie für die nachfolgende Kopplungsreaktion vorzubereiten.
3. Kopplungsreaktion: Der Thiol(-SH)-konjugierte Antikörper wird mit LNP in einem geeigneten Puffer (z. B. PBS, pH 7,4) bei niedriger Temperatur (z. B. 4 °C) inkubiert (üblicherweise mehrere Stunden bis über Nacht). Die Thiolgruppen des Antikörpers binden kovalent an die Maleimid(-MAL)-Gruppen auf der Oberfläche der LNP und schließen so die gezielte Funktionalisierung ab.
Im Vergleich zu viralen Vektoren wie Lentiviren und adeno-assoziierten Viren bietet das auf DSPE-PEG-MAL basierende LNP-Verabreichungssystem Vorteile wie geringe Immunogenität, kein Risiko von Insertionsmutationen und einfache Massenproduktion, was es zu einem idealen Vektor für CAR-T in vivo macht.
Die wichtigsten Vorteile von SINOPEGs GMP-konformem DSPE-PEG-MAL
GMP-konforme Produktion und sofortige Lieferung
In der aktuellen Forschungs- und Entwicklungsphase der In-vivo-CAR-T-Zelltherapie sind hochwertige und stabil verfügbare Hilfsstoffe die Grundlage für einen reibungslosen Forschungs- und Entwicklungsfortschritt. Xiamen SINOPEGe hat ein umfassendes GMP-Qualitätsmanagementsystem etabliert, die GMP-konforme Großproduktion von DSPE-PEG-MAL erfolgreich aufgenommen und einen ausreichenden Lagerbestand aufgebaut.
Die Doppelanmeldung für CDE und DMF steht kurz vor dem Abschluss.
Um Kunden bei Zulassungsanträgen für Arzneimittel besser zu unterstützen, wird unser Produkt DSPE-PEG-MAL aktiv beworben:
• Registrierung und Einreichung von Hilfsstoffen für die chinesische Arzneimittelzulassungsbehörde (CDE): Nach Abschluss kann die Registrierung direkt mit Anträgen auf Arzneimittelzulassung verknüpft werden.
• FDA-DMF-Einreichung in den Vereinigten Staaten: Bietet eine maßgebliche Grundlage für den Nachweis der Qualität und Konformität von Hilfsstoffen gegenüber der FDA.
SINOPEG hat ein umfassendes Qualitätskontrollsystem etabliert, das von der Rohstoffbeschaffung über die Syntheseprozesse bis hin zur Reinigung reicht. Wir sind uns bewusst, dass bei innovativen Therapien wie der In-vivo-CAR-T-Zelltherapie selbst geringfügige Unterschiede bei den Hilfsstoffen erhebliche Auswirkungen auf die physikochemischen Eigenschaften, das In-vivo-Verhalten und sogar die therapeutische Wirkung der finalen Formulierung haben können. Wir kontrollieren nicht nur streng die Reinheit, die Aktivität der Maleimid-Gruppe (-MAL) und die Integrität der PEG-Kette, sondern haben basierend auf unserem fundierten Wissen über die industrielle Produktion von PEG und Wirkstoffderivaten sowie unserer Erfahrung mit zahlreichen IND-Anträgen eine Reihe spezifischer Charakterisierungstests entwickelt. Die differenzierten Vorteile dieser detaillierten physikochemischen Charakterisierungen liefern umfassendere Daten für Ihren Projektantrag. Nach Abschluss der Doppelregistrierung können Kunden direkt unsere Registrierungsnummer verwenden. Dies vereinfacht den IND- (New Drug Clinical Trial Application) oder NDA-Antrag (New Drug Marketing Application) erheblich, spart Zeit und Arbeitskosten und erhöht die Erfolgsquote Ihrer Projektanträge deutlich.
Erweiterung der DSPE-PEG-Produktreihe
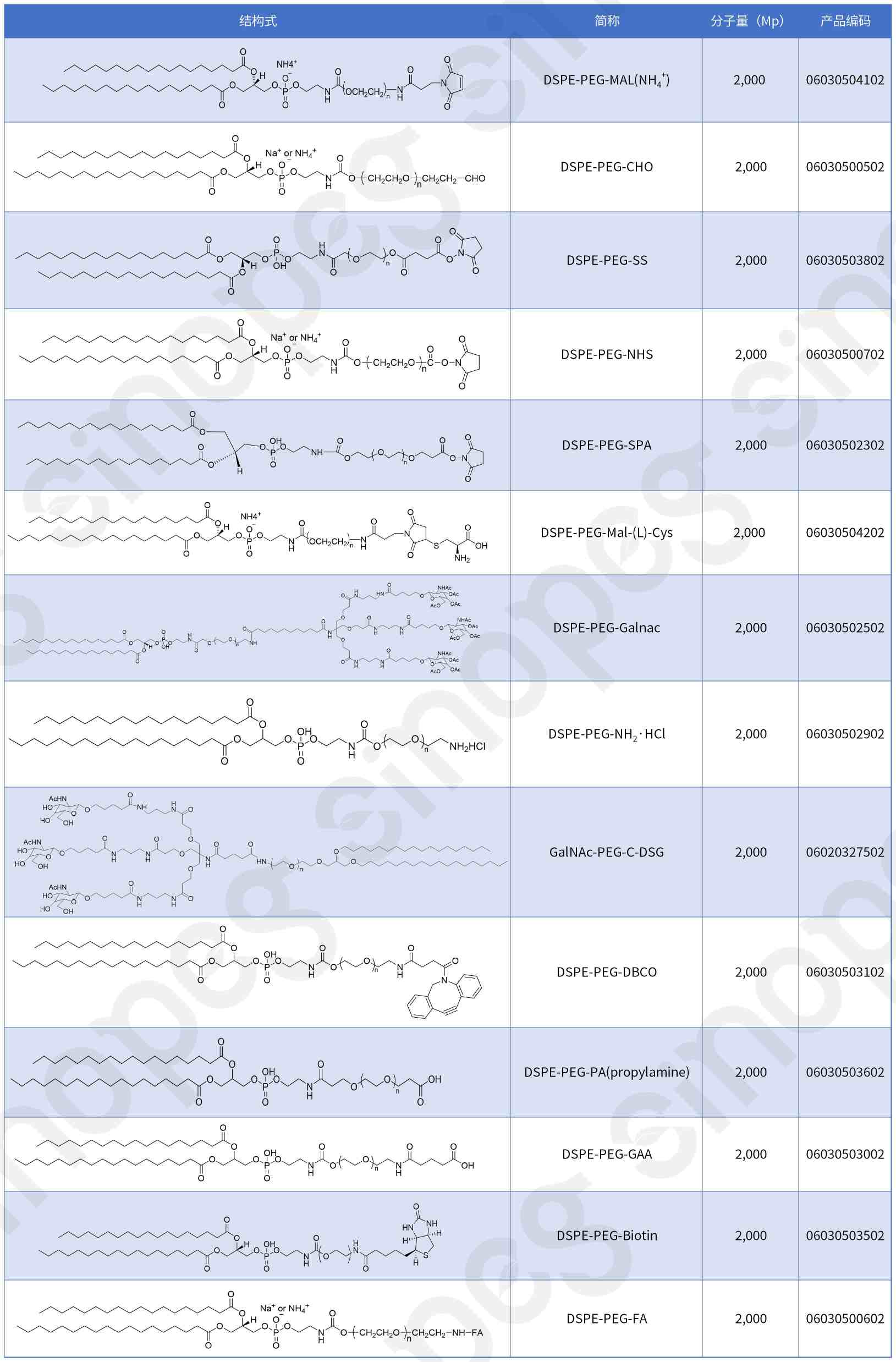
Neben DSPE-PEG-MAL bietet unser Unternehmen auch kundenspezifische Entwicklungsdienstleistungen für eine Vielzahl funktionalisierter Phospholipid-PEG-Derivate an, um unterschiedlichen F&E-Anforderungen gerecht zu werden.
Referenz:
1. Capstan Therapeutics. Capstan Therapeutics gibt den Beginn der Phase-1-Studie mit dem führenden In-vivo-CAR-T-Zelltherapie-Kandidaten CPTX2309 zur Behandlung von Autoimmunerkrankungen bekannt. Business Wire. 11. Juni 2025.
2. AbbVie. AbbVie übernimmt Capstan Therapeutics und stärkt damit sein Engagement für die Verbesserung der Patientenversorgung in der Immunologie. AbbVie News Center. 30. Juni 2025.
3. Amerikanische Gesellschaft für Klinische Onkologie. CAR-T-Zelltherapie: Kosten und Überlegungen. Tagungsband der ASCO-Jahrestagung. 2024.
4. Smith J, et al. In vivo CAR-T-Zellen zeigen eine starke Antitumoraktivität bei reduzierter Herstellungskomplexität. Nature Biotechnology. 2023;41(5):678-685.
5. Wang D, et al. Gezielte Lipidnanopartikel für das T-Zell-Engineering in vivo. Science Advances. 2024;10(12):eadl2165.
6. Chen X, et al. Antikörper-konjugierte LNP für die präzise In-vivo-Genübertragung in T-Zellen. Cell Reports Medicine. 2024;5(3):101489.
7. Zhang Y, et al. Molekulare Struktur und Membranverankerungseigenschaften von DSPE-PEG-Lipiden. Biochimica et Biophysica Acta. 2023;1865(4):184321.
8. Gabizon A, et al. Verlängerte Zirkulationszeit und erhöhte Anreicherung von in Polyethylenglykol-beschichteten Liposomen verkapseltem Doxorubicin in malignen Exsudaten. Cancer Research. 1994;54:987-992.
9. Hermanson GT. Biokonjugationstechniken. 3. Aufl. Academic Press; 2021.
10. Wei X, et al. Mikrofluidische Synthese von zielgerichteten Lipidnanopartikeln für das T-Zell-Engineering. Lab on a Chip. 2024;24(8):2156-2168.
11. Kato T, et al. Effiziente Antikörperkonjugation mit Trauts Reagenz zur Funktionalisierung von LNP. Bioconjugate Chemistry. 2023;34(7):1256-1265.
12. Li M, et al. Kovalente Konjugation von Antikörpern an die Oberfläche von LNP zur gezielten Wirkstofffreisetzung. Journal of Controlled Release. 2024;368:456-467.
13. Xu Q, et al. Nicht-virale Verabreichungssysteme für das In-vivo-CAR-T-Zell-Engineering. Nature Reviews Materials. 2024;9(3):189-205.