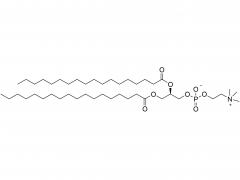
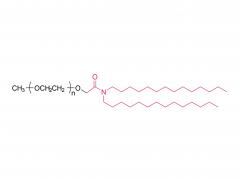
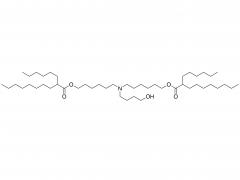
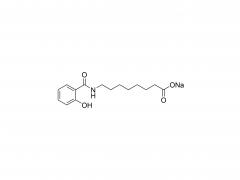
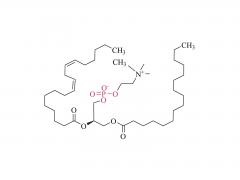
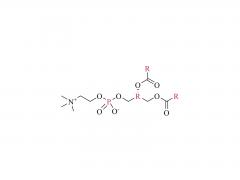
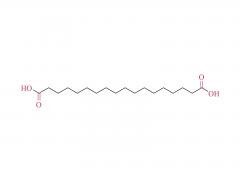
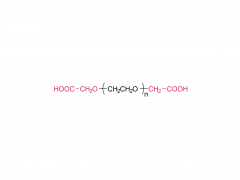
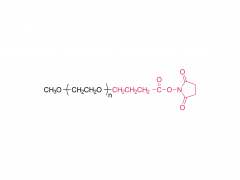
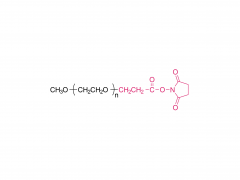
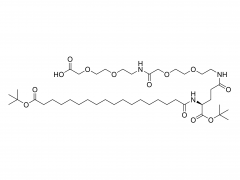
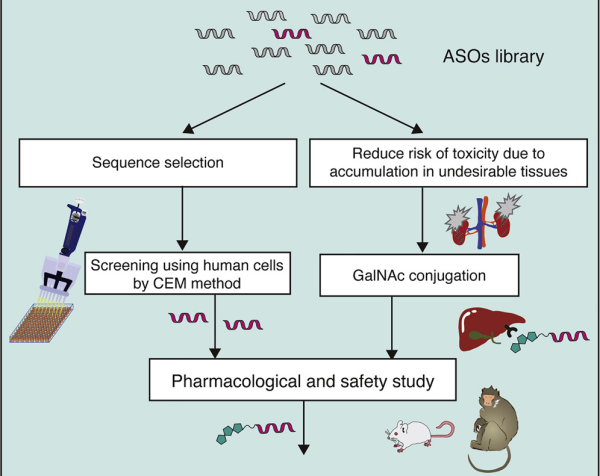
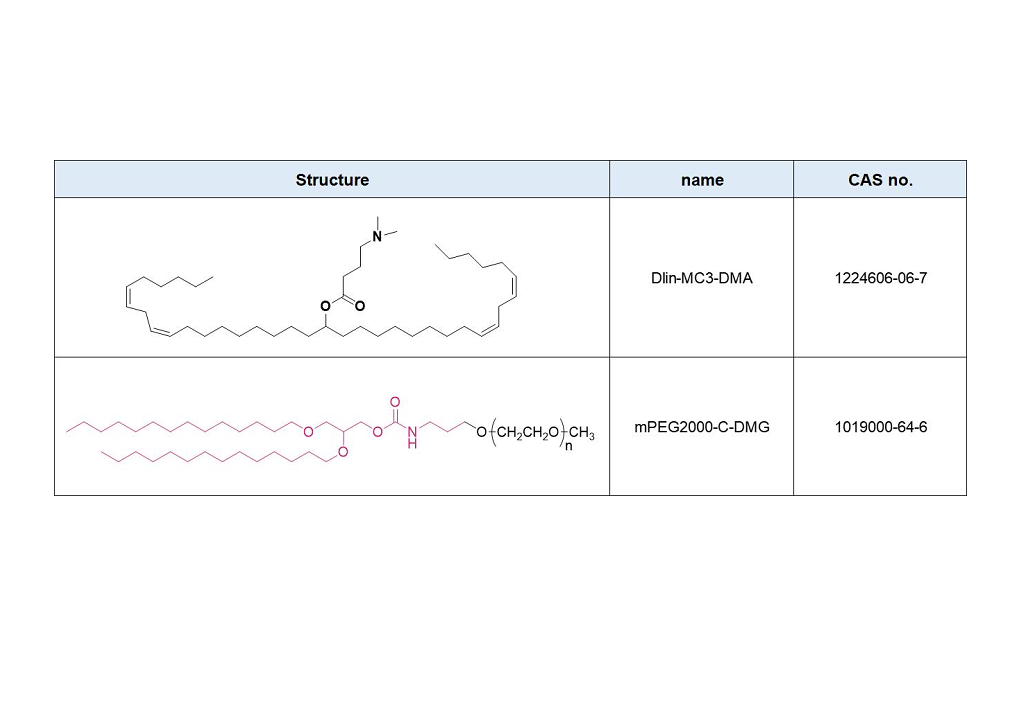
#ASOs #Antisense-Oligonukleotide #GalNAc #Wirkstofftransport #Liganden-Targeting Das Arzneimittelentwicklungsschema unter Verwendung des GalNAc-Konjugats ist besser geeignet für die Auswahl von ASOs auf BNA-Basis, insbesondere für die Behandlung von Leber-assoziierten Erkrankungen. gnade https://www.cell.com/molecular-therapy-family/molecular-therapy/fulltext/S1525-0016(22)00428-2 Antisense-Oligonukleotide (ASOs), die verbrückte Nukleinsäuren (BNAs) enthalten, haben sich als sehr wirksam erwiesen. Es besteht jedoch noch immer die Herausforderung, ein zuverlässiges Entdeckungs- und translationales Entwicklungsschema für diese Klasse von ASOs mit breiteren therapeutischen Fenstern sicherzustellen. Die Robustheit des Schemas wurde im Zusammenhang mit der Auswahl von ASOs demonstriert, die zwei unterschiedliche BNA-Chemien (2,′4′-BNA/Locked Nucleinsäure [LNA] und Amido-verbrückte Nucleinsäure [AmNA]) aufweisen, die auf menschliches Proprotein abzielen Konvertase Subtilisin/Kexin Typ 9 (PCSK9). Ein zweistufiger Prozess wurde vorgestellt, einschließlich eines einzigartigen und empfindlichen In-vitro-Screening-Ansatzes, der als Ca2+-Anreicherung des Mediums (CEM) Transfektion bezeichnet wird, und eines Liganden-gerichteten Ansatzes zur Arzneimittelabgabe, um Zielgewebe besser zu erreichen und eine unbeabsichtigte Anhäufung von ASOs abzuwenden. Anschließend wurde ein N-Acetylgalactosamin (GalNAc)-Ligand an das Kandidaten-ASO angehängt, um den therapeutischen Spielraum durch Veränderung der Pharmakokinetik des Moleküls weiter zu erweitern. Bei reduzierter Nephrotoxizität bei Ratten erwies sich das GalNAc-Konjugat, HsPCSK9-1811-LNA, bei nichtmenschlichen Primaten als mindestens zehnmal wirksamer. Insgesamt erwies sich ein Arzneimittelentwicklungsschema als besser geeignet für die Auswahl klinisch relevanter BNA-basierter ASOs, insbesondere für die Behandlung von Lebererkrankungen.
mehr sehen