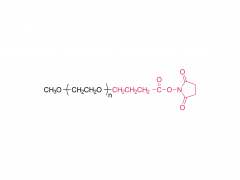
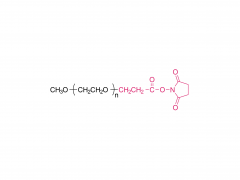
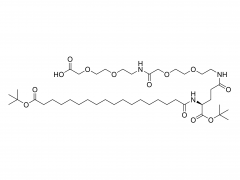
Bioact Mater. 2024 Jun 21:40:430-444. doi: 10.1016/j.bioactmat.2024.06.021. eCollection 2024 Oct. Knetbares, teigartiges Hydrogel, das sich von einem dynamischen in ein starres Netzwerk umwandelt, um unregelmäßige Knochendefekte zu reparieren Abstrakt Unregelmäßige Knochendefekte, die sich durch unvorhersehbare Größe, Form und Tiefe auszeichnen, stellen eine große Herausforderung für die klinische Behandlung dar. Obwohl verschiedene Knochentransplantate verfügbar sind, kann keines den Reparaturbedarf des Defektbereichs vollständig decken. In dieser Studie wird ein teigartiges Hydrogel (DR-Net) hergestellt, dessen erstes dynamisches Netzwerk durch die Koordination von Thiolgruppen und Silberionen gebildet wird. Dadurch ist es knetbar und passt sich verschiedenen unregelmäßigen Knochendefekten an. Das zweite starre kovalente Netzwerk entsteht durch Photovernetzung, wodurch der osteogene Raum unter äußeren Kräften erhalten bleibt und eine bessere Anpassung an den Knochenregenerationsprozess erreicht wird. In vitro wurde ein unregelmäßiger Alveolarknochendefekt im frischen Schweineunterkiefer erzeugt. Das teigartige Hydrogel zeigte eine hervorragende Formanpassungsfähigkeit und passte sich perfekt der Morphologie des Knochendefekts an. Nach der Photohärtung erhöhte sich der Speichermodul des Hydrogels um das 8,6-Fache, von 3,7 kPa (vor der Bestrahlung) auf 32 kPa (nach der Bestrahlung). Darüber hinaus ermöglicht dieses Hydrogel die effektive Beladung mit dem P24-Peptid, welches die Knochenheilung bei Sprague-Dawley-Ratten mit kritischen Schädeldefekten wirksam beschleunigt. Insgesamt zeigt das teigartige Hydrogel mit Knetbarkeit, raumerhaltender Wirkung und osteogener Aktivität ein außergewöhnliches Potenzial für die klinische Anwendung zur Behandlung unregelmäßiger Knochendefekte. Schlüsselwörter: Teigartiges Hydrogel; Dynamisches Netzwerk; Unregelmäßiger Knochendefekt; Knetbar; Starres Netzwerk. Produkt: Hersteller von PEG-Derivaten nach Struktur, Großhandel mit PEG-Derivaten nach Struktur
mehr sehen