Mechanisches Tempern löst das piezoelektrische Aminosäure-Puzzle! Die Universität Nanjing entwickelt biologisch abbaubare piezoelektrische Kraftsensoren
August 7,2025.
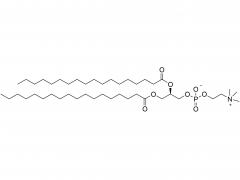
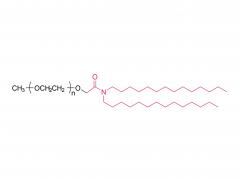
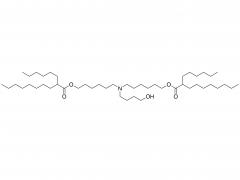
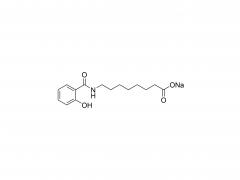
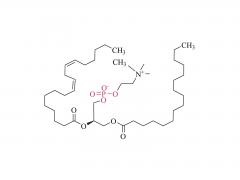
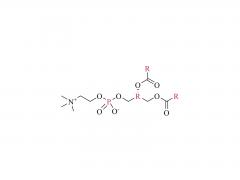
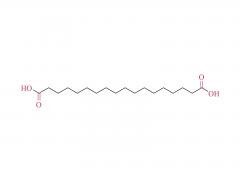
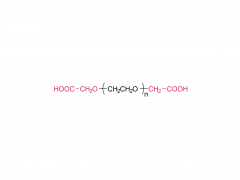
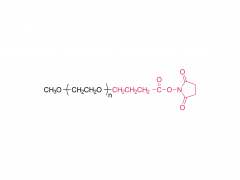
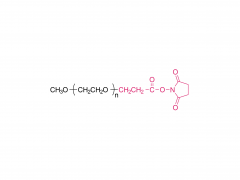
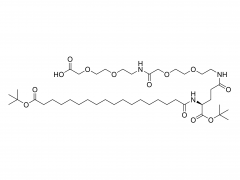
Stellen Sie sich winzige piezoelektrische Kraftsensoren vor, die im Körper platziert werden können: Sie überwachen physiologische Druckänderungen in geschädigten Organen, unterstützen die präzise Verabreichung von Medikamenten oder fördern die Reparatur und Regeneration von Gewebe. Und das Beste daran? Sie benötigen keine Batterieleistung und nach Gebrauch der Körper absorbiert und baut sie ab , wodurch eine invasive Entfernungsoperation überflüssig wird! Traditionelle piezoelektrische Materialien wie anorganische Keramiken und organische Polymere weisen jedoch eine unzureichende Abbaubarkeit und Zytotoxizität auf. Wissenschaftler identifizierten Aminosäurekristalle als vielversprechende Kandidaten – sie sind biokompatibel und Ausstellung ausgezeichnete piezoelektrische Eigenschaften Die Herausforderung? Diese Kristalle sind zu klein, wie verstreuter Sand, was es äußerst schwierig macht, sie zu funktionsfähigen Geräten auszurichten. Die Forscher Yi Cao und Bin Xue von der Universität Nanjing haben eine Lösung gefunden: eine spezielle Technik namens „ Mechanisches Glühen „. Unter Verwendung natürlicher Aminosäurekristalle als piezoelektrisches Material entwickelten sie vollständig organische, biologisch abbaubare piezoelektrische Kraftsensoren. Durch mechanisches Glühen stieg die Stromerzeugungsfähigkeit der Kristalle sprunghaft an – sie erreichten einen 12-mal höheren piezoelektrischen Koeffizienten als Einkristallpulver! Darüber hinaus wurden die behandelten Kristallfilme glatt und flach, wie ein Displayschutz für Mobiltelefone, was den Kontakt mit den Elektroden deutlich verbesserte und stärkere, stabilere elektrische Signale ermöglichte. Das Ergebnis " absorbierbare piezoelektrische Kraftsensoren ", wurden nach der Verpackung in vivo implantiert und überwachten erfolgreich dynamische Bewegungen wie Muskelkontraktionen und Lungenatmung kontinuierlich für 4 Wochen . Danach allmählich abgebaut, ohne Entzündungen oder systemische Toxizität zu verursachen . Dieser Durchbruch bietet neue Hoffnung für die Medizin der Zukunft und bietet einen Weg zur Entwicklung und Herstellung vollständig organischer, biologisch abbaubarer Kraftsensoren für potenzielle klinische Anwendungen! Herstellung des verpackten Kraftsensors: Herstellung mechanisch getemperter Kristallfilme: Isoleucin wurde in deionisiertem Wasser gelöst, erhitzt und anschließend in ein Eiswasserbad gegeben, wo es stehen blieb, damit sich Kristallkeime bilden konnten. Die Kristalle wurden anschließend gesammelt und im Ofen getrocknet. Die hergestellten Isoleucinkristalle wurden in eine Tablettenform gefüllt und einem mechanischen Glühprozess unterzogen, wodurch runde, filmartige Kristalle entstanden. Andere Aminosäurekristalle und ihre mechanisch geglühten Gegenstücke wurden mit der gleichen Methode hergestellt. Vorbereitung der PLA-PAN-Elektrode: Polymilchsäure (PLA) wurde in Dichlormethan (DCM) gelöst, um PLA-Filme zu bilden, die als äußere „Schutzmembran“ des Sensors dienen. Doch eine Membra...
mehr sehen